エンプラ事業
すべてのキーモノマーをサステナブルに
当社は、過去にバイオマス由来のキーモノマーを活用したLAPEROS® LCP をご紹介しましたが、今回はLCPのもう一つの重要なキーモノマーについても、サステナブル素材の活用を検討し始めましたのでご紹介します。
これまで、主に狭ピッチコネクタなどに用いられるLCPのグレードはナフタレン由来のモノマーが多く使用されています。ナフタレンは、石炭を高温で燃焼させて得られるコークス製造時に発生するコールタールに含有されるものです。しかし、石炭は燃焼時にCO₂を発生するため環境負荷が高く、当該モノマーのサステナブル化は重要な課題でした。LCPの原料をすべてサステナブルなものにしていくためには、ナフタレン由来のモノマーをサステナブル化できるかどうかが重要なカギとなるのです。
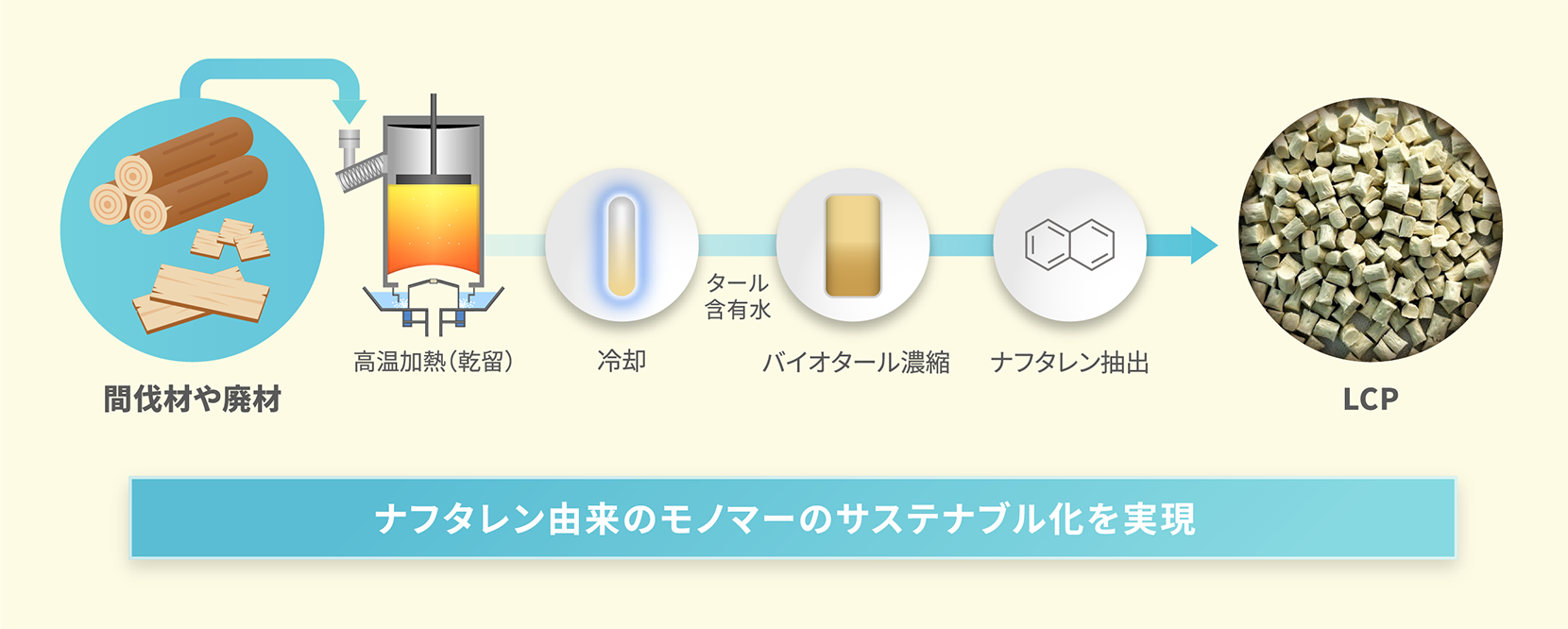

そこで、当社が目を付けたのが日本で古くから受け継がれてきた「炭焼き」工程です。炭は木材を炭焼き窯で高温加熱(乾留)することで得られますが、その際に発生するガス成分を冷却して木タール(バイオタール)を得ることができます。間伐材や廃材から資源を再利用することができるため環境に優しく、またこのバイオタールからナフタレンを抽出することが可能です。まさにサステナブルな素材としての救世主でした。
パルプの廃液成分の活用も視野に
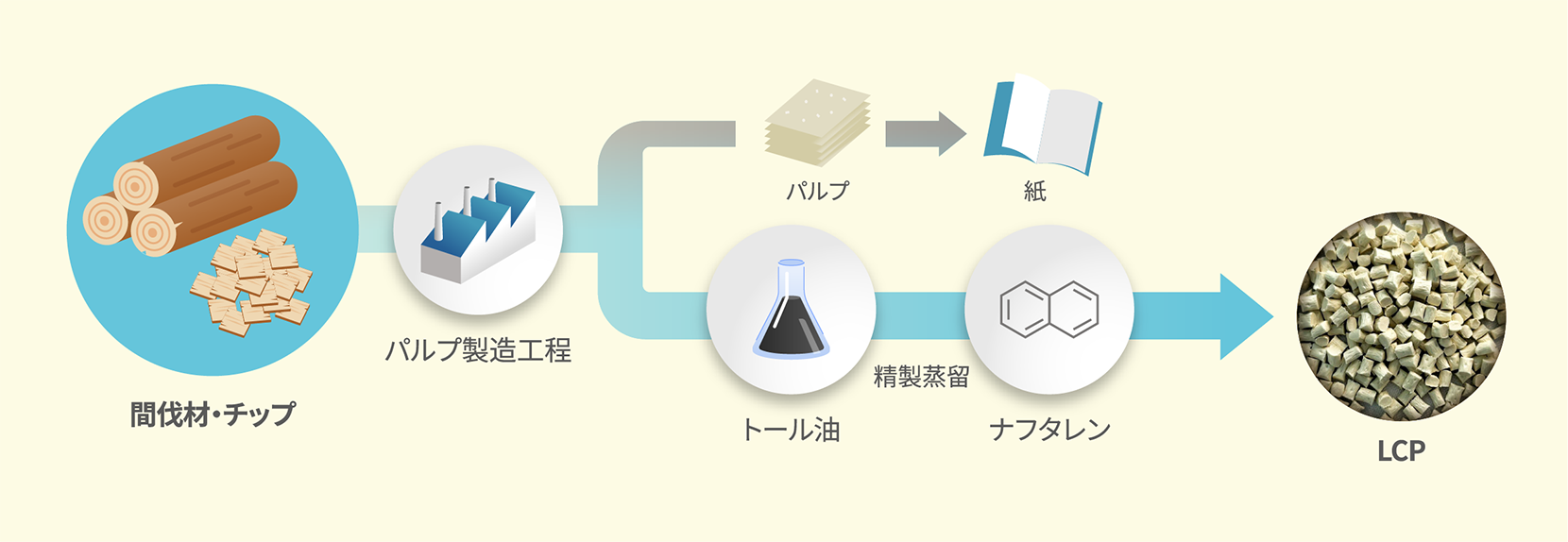

バイオタールのほかに、パルプの製造工程で発生する廃液からナフタレンを取り出す方法も検討しています。バイオタールよりも多くの量のナフタレンを確保することができる可能性があるだけでなく、本来処分されるはずの資源を有効活用できるという点も環境配慮に適しているといえます。
原料のサステナブル化を目指すLCPのグレードは、優れた薄肉性、高流動性を持ち、狭ピッチコネクタなどに用いられます。この狭ピッチコネクタは、各種モバイル機器向けを始めウェアラブル端末や車載用インバータ、コンバータ、電池監視システム、さらには半導体やプリント基板の検査用プローブカードなどに不可欠であり、これからの産業の発展に重要な素材です。そのような素材を支えるLCPのグレードが、お客様の環境へのニーズに応えながら未来社会の更なる発展を支えることができるのです。
当社は、今後もすべての樹脂において環境配慮製品の開発を進め、エンプラのリーディングカンパニーとして包括的な環境ソリューションを提供していきます。
ナフサを得る新たな発酵技術も
株式会社ダイセルは、優れた発酵技術を有する会社です。糖を原料とし特定の菌を用いて、低環境負荷の発酵プロセスによりLCPモノマーをつくり出す検討を当社と共同でスタートしました。ダイセルグループの力を結集してLCPモノマーの更なるサステナブル化も可能になります。
関連記事はこちら
DURACON® POM短繊維セルロース強化グレードの開発
循環型社会の実現に向けて環境負荷が低い素材が注目され、中でも植物由来のセルロースの可能性が期待されています。当社でも、お客様の環境ニーズに応える製品として、DURACON® POM短繊維セルロース強化グレードの開発を開始しました。
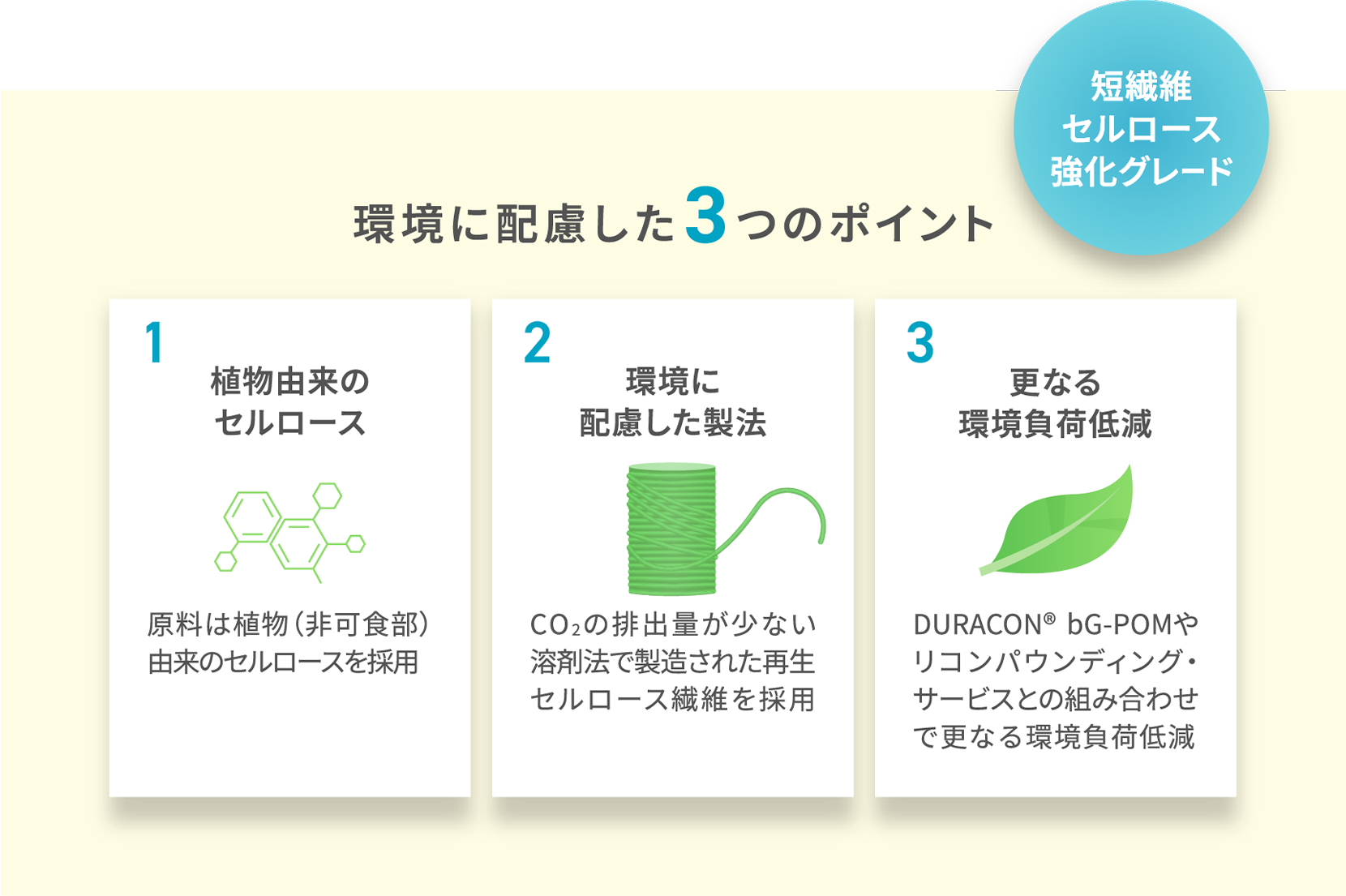
一般的にセルロースは、再生可能な繊維の一種で枯渇の心配がないため強化材として樹脂に配合することで製品のライフサイクル全体のCO2排出量を削減することが可能になります。今回開発を進めているグレードは、廃棄物をほとんど発生させない溶剤法で製造された再生セルロース繊維を使用するため、製造過程においてもCO2の排出量を削減することができます。加えて、この再生セルロース繊維は非可食部由来のものであるため、資源の有効活用という観点からも環境負荷の低減に寄与します。
さらに、当社が展開するサステナブルな原料を活用したDURACON® bG-POMや、エンプラリサイクルをコンセプトとするリコンパウンディング・サービスとの組み合わせにより、一層の環境負荷の低減が期待できるのです。

機能面では、POM本来の優れた摺動特性を維持している点が大きな特長です。POMをガラス繊維で強化したグレードと比較した場合、ガラス繊維は摺動時に相手材を摩耗させてしまう傾向にあり、高い機械物性と良好な摺動特性を両立させることが難しいとされています。しかし、セルロース繊維は優れた摺動特性だけでなく高剛性も両立させることが可能です。また、セルロース量を増やすことでガラス繊維強化POMに匹敵する程度の弾性率を実現することができます。
当グレードは、従来のPOMと同様に自動車のドアロック・ドアクラッチ、シートベルトロック機構などの安全部品から、歯車やねじ、軸受けといった機械要素部品、ファスナーや歯ブラシの柄などの生活用品、更にはPCキーボード部品などの幅広い用途に使用されることが期待されます。
当社は、循環型社会の実現に向けて、機能性(製品ニーズ)と環境性(環境ニーズ)を両立した高付加価値な樹脂開発によって画期的なエンプラソリューションを提供していきます。
アルミレスPTPシートの開発でモノマテリアル化を実現
近年、循環型社会の実現に向けてリサイクルニーズが急速に高まっており、そのような中でモノマテリアルの製品が注目されています。当社もモノマテリアルに貢献する製品として、この度 TOPAS® COC を活用したPTPシートのアルミレス化を実現しました。
従来のPTPシートは、錠剤やカプセルなどの薬をプラスチックとアルミ箔の2種類で包んでいるものが多いのですが、リサイクルをする際には各素材を分離することが難しく、結果としてリサイクルされず廃棄されてしまい環境への負荷が大きくなってしまう懸念があります。これらの課題を解決すべく、当社はCOCを活用したアルミレスPTPシートを開発しました。
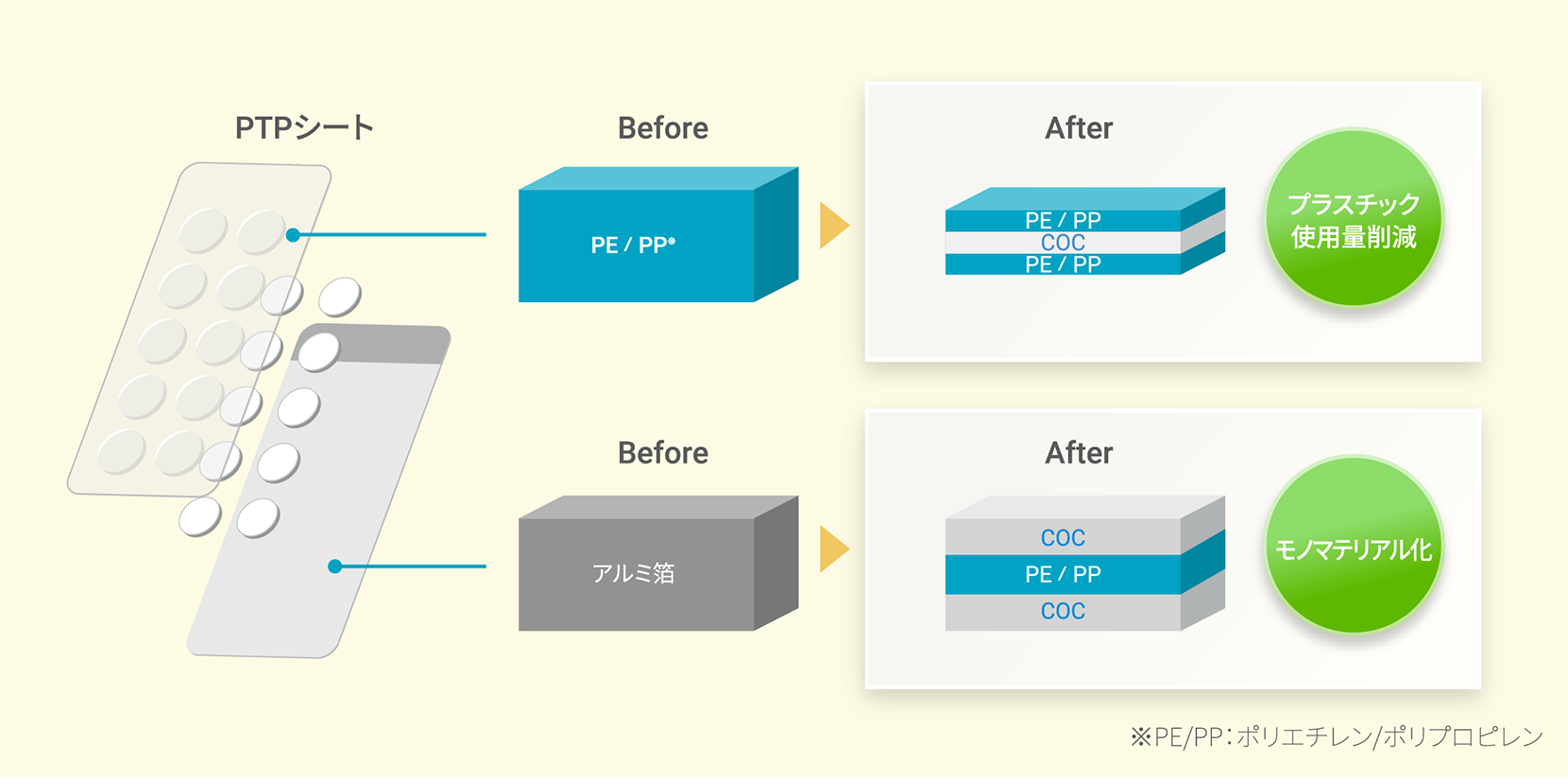
耐薬品性や安全性に優れ、医療・薬品分野、包装分野で用途を展開するCOCはオレフィン系樹脂との親和性に優れることから、PTPシートの従来素材であるポリエチレンやポリプロピレンと一緒に処分することが可能となります。また、COCはオレフィン系樹脂と複合化するとフィルムが脆性的になる特性を持つため、PTPシートに使われているアルミ箔の代替フィルムとして使用でき、単一(モノ)素材としてのリサイクルを実現します。このモノマテリアル化は、リサイクル工程においても異素材の混入を限りなく少なくできるため、品質向上にもつながります。
さらに、COCとオレフィン系樹脂の複合化は水蒸気バリヤ性の向上をもたらし、薄肉化を可能にします。それにより、プラスチックの使用量を削減することにもつながるのです。

アルミレスPTPシートは、循環型社会の実現に大きく寄与するとともに製品品質(機能面)の向上にもつながるものです。その他のモノマテリアル包装においても、COCの添加、複合化によりポリエチレンやポリプロピレンの剛性、バリヤ性などの機能を向上させることができるため、さまざまな包装に適用が始まっています。今後も機能性と環境性を両立した高付加価値な樹脂開発に取り組みます。
関連記事はこちら
製品ニーズと環境ニーズに同時に応える
プラストロン® LFTセルロース繊維強化グレードの開発
浅川組運輸様は、港運事業に加え陸上貨物運送や倉庫、包装など総合的な物流サービスを提供している企業です。この度、浅川組運輸様のエムネジに当社のプラストロン® LFTセルロース繊維強化グレードが採用されました。
エムネジは、輸送用の強化段ボールを留める樹脂製の梱包資材です。金属製の留め具は、取り付ける機具が限定され熟練された作業が求められる場合もありますが、エムネジは電動ドライバーなどで簡単に取り付けができるため作業効率を高めることができます。また、ネジの先端が飛び出ることがないため作業時や輸送時の安全性にも考慮された製品です。
近年、梱包資材についても環境負荷低減に資する素材などが求められており、十分な強度があり、かつバイオマス素材という両方の特性を備える当社のLFTセルロース繊維強化グレードが採用されました。

輸送用の梱包資材は、輸出時に使用されるケースもあり、厳しい物流環境下で耐えることのできる強度が求められます。この度採用された当社セルロース繊維入り強化グレードのセルロース繊維は、長繊維であるためより高い衝撃強度や高い剛性を出すことができます。
環境面では、このセルロース繊維は植物由来のサステナブルな素材であり、さらに焼却時はガラス繊維や金属と異なり残渣が発生しないため産業廃棄物削減につながる「サーマルリサイクル」を可能にします。また、エムネジの一般グレードで使用されているナイロン樹脂と比べても製造時のエネルギー消費が少ないためプロダクトカーボンフットプリントも低く、さらに本グレードは軽量であるため副資材的な観点からみても輸送時のCO₂削減の貢献につながります。
当社は、LFTのベース樹脂にPCR材を使用したグレードを検討するなど、更なる環境配慮製品の開発を進めています。
浅川組運輸様よりコメント
当社は、“エムネジ”にバイオマス素材を配合することに数年間取り組んできました。一般的にバイオマス素材の配合率を上げると製品強度が低下しますが、プラストロン® LFTセルロース繊維強化グレードを採用することにより強度を確保した環境配慮製品を開発することができました。今後は、ポリプラスチックス株式会社様のPCR材を使用したグレードに期待しております。


